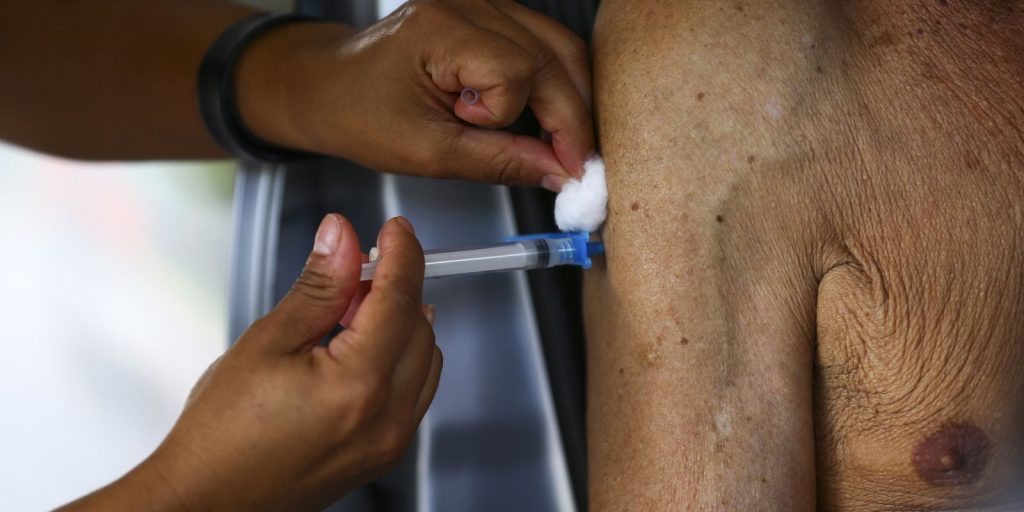
A vacina aprovada, denominada Arexvy, é produzida pela empresa GlaxoSmith Kline e tem como público-alvo os adultos com 60 anos de idade ou mais. O imunizante é administrado por via intramuscular, em dose única, e conta com a tecnologia de proteína recombinante. Nesse processo, uma substância semelhante à encontrada na superfície do vírus é produzida em laboratório e utilizada para estimular a produção de anticorpos, promovendo a imunidade.
A aprovação da vacina foi classificada como prioritária pela Anvisa, conforme estabelecido na Resolução da Diretoria Colegiada (RDC) 204/2017. A agência destacou a gravidade e a debilitação causada pela condição, assim como o impacto significativo da doença na saúde pública, especialmente devido ao alto índice de hospitalizações resultantes de infecções pelo VSR em pacientes na faixa etária contemplada pela vacina.
Segundo a Anvisa, a aprovação do registro do Arexvy representa um avanço significativo no combate e prevenção da doença do trato respiratório inferior causada pelo VSR, oferecendo uma nova opção terapêutica para a população de idosos, que é particularmente vulnerável a complicações decorrentes da infecção pelo vírus.
No entanto, a agência ressalta a importância da continuidade das medidas de prevenção e proteção, como a vacinação em dia, a higienização frequente das mãos e a adoção de práticas de distanciamento social, especialmente em meio à atual pandemia de COVID-19.
A aprovação do registro da vacina Arexvy pela Anvisa representa um marco importante para a saúde pública e reforça o compromisso em oferecer soluções eficazes para o enfrentamento de doenças respiratórias, especialmente em grupos de maior risco.